Pada tahun 1950-an, thalidomide merupakan bahan kimia yang digunakan sebagai ubat untuk ibu mengandung mengurangkan mabuk ketika hamil. Namun sewaktu kelahiran, didapati anak tersebut mengalami kecacatan! Kisah penggunaan ubat bernama thalidomide ini pastinya menjadi rujukan klasik berkenaan stereokimia.
Pengetahuan berkenaan stereokimia yang melibatkan penyusunan atom dalam ruang tiga dimensi adalah penting dalam pembentukan struktur molekul sebatian kimia. Penyusunan atom yang berbeza bagi sebatian kimia yang mempunyai formula molekul yang sama, akan menghasilkan sebatian berbeza yang dikenali sebagai isomer.
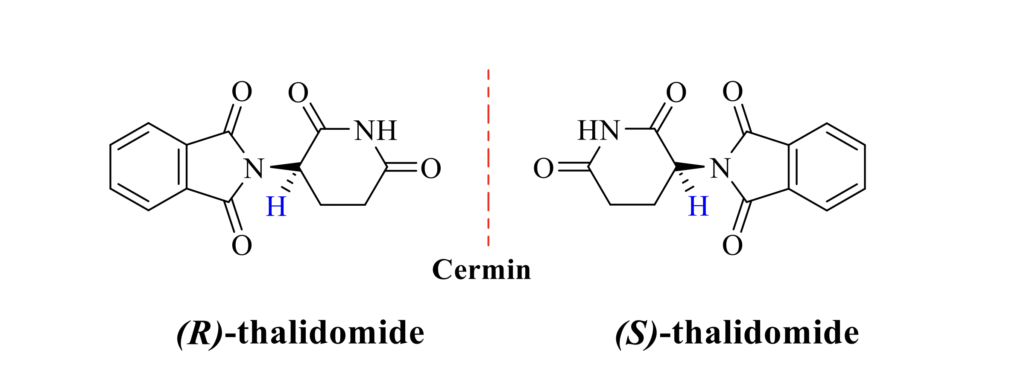
Kajian saintifik lanjutan mendapati thalidomide mempunyai isomer dengan dua sebatian berbeza yang merupakan imej cermin antara satu sama lain. Satu daripada isomernya sangat berkesan untuk mengurangkan mabuk kehamilan. Walau bagaimanapun, satu lagi isomer cerminannya boleh menyebabkan kecacatan kepada bayi!
Kewujudan dua isomer thalidomide tersebut boleh diibaratkan sama dengan dua tangan manusia. Kita tahu bahawa tangan kanan adalah cerminan kepada tangan kiri jika diletakkan secara bertentangan berhadapan dengan satah cermin. Kita dapati, ibu jari kanan akan bertemu dengan ibu jari kiri dan jari kelingking kanan akan bertemu dengan jari kelingking yang kiri. Sama bukan?

Namun begitu, jika diletakkan tangan kanan di atas tangan kiri pada arah yang sama, tentunya jari yang sama tidak akan bertemu. Misalnya ibu jari tangan kanan akan bertemu jari kelingking tangan kiri pula. Walaupun dipusing pada pelbagai arah, pastinya kedua-dua belah jari tangan tidak akan bertemu. Inilah yang dinamakan isomer cermin!
Konsep yang sama turut digunakan pada pelbagai sebatian kimia termasuk thalidomide. Terdapat pelbagai lagi sebatian yang mempunyai isomer cermin dengan pelbagai manfaat terutamanya dalam industri perubatan, perisa dan pewangi.
Secara saintifik, isomer ini juga dikenali sebagai isomer optik. Ini terjadi apabila dua sebatian kimia organik mempunyai bilangan dan jenis atom dengan formula molekul yang sama, dengan kedua-duanya adalah imej cerminan. Isomer optik ini perlu mempunyai sekurang-kurangnya satu atom karbon yang mempunyai empat kumpulan penukarganti yang berbeza yang dikenali sebagai karbon tidak simetri ataupun karbon kiral. Contohnya sebatian 2-butanol.
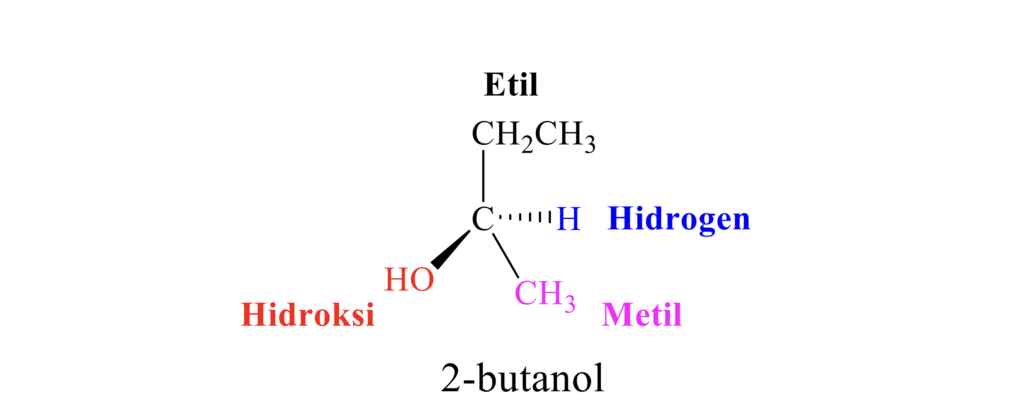
Bagi sebatian 2-butanol, atom karbon ini merupakan karbon kiral kerana ianya terikat dengan empat kumpulan berbeza iaitu hidroksi, etil, metil dan hidrogen. Dalam ruang tiga dimensi, isomer ini boleh dikelaskan berdasarkan penyusunan empat kumpulan berbeza tersebut. Keutamaan diberikan kepada kumpulan yang mempunyai nombor atom yang paling besar dan kumpulan paling kurang keutamaan adalah kumpulan yang mempunyai nombor atom yang paling kecil yang diletak pada arah belakang.
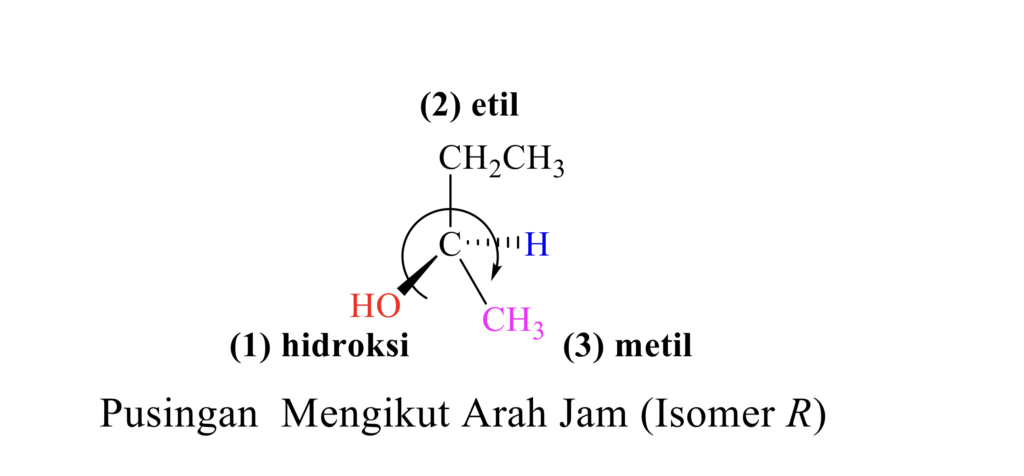
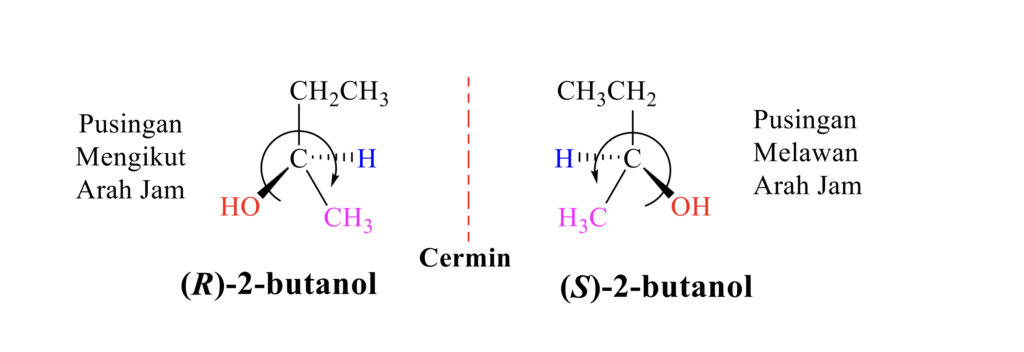
Dalam contoh 2-butanol, kumpulan yang paling utama adalah hidroksi (1) kerana mempunyai nombor atom yang paling besar dan diikuti dengan etil (2), metil (3) dan hidrogen (4) yang mempunyai nombor atom yang paling kecil. Disebabkan hidrogen adalah yang paling kurang keutamaan, ia disusun pada arah belakang. Jika pusingan keutamaan yang bermula daripada hidroksi, kemudian etil dan diakhiri dengan metil adalah mengikut arah jam, maka isomer tersebut dikelaskan sebagai jenis (R). Sebaliknya jika pusingan keutamaan melawan arah jam, maka isomer tersebut adalah kelas (S).
Thalidomide juga mempunyai dua isomer iaitu (R)-thalidomide dan (S)-thalidomide dengan kesan yang berbeza seperti yang dibincangkan. Dalam industri perubatan, adakalanya campuran kedua-dua sebatian berupaya meningkatkan kesan positif perubatan. Walau bagaimanapun, thalidomide, perkara sebaliknya telah berlaku dengan kewujudan (S)-thalidomide yang boleh menyebabkan kecacatan kepada bayi.
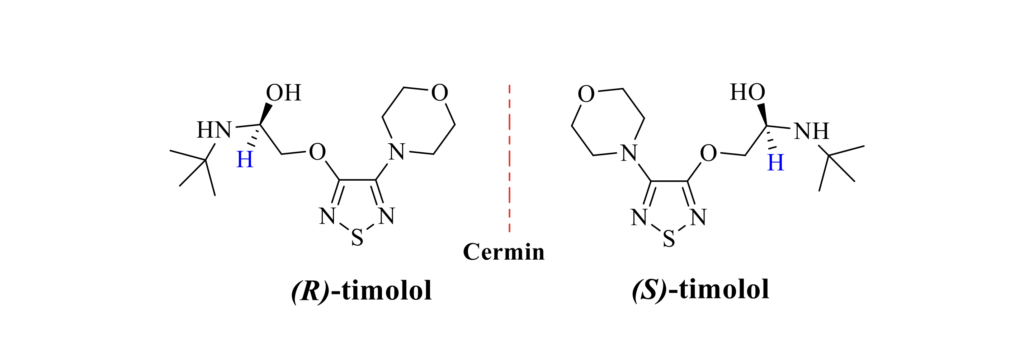
Dalam kes yang lain pula, isomer yang berbeza secara optik boleh juga memberikan kesan perubatan yang berbeza. Misalnya, ubat (S)-timolol digunakan untuk merawat tekanan darah tinggi. Manakala, (R)-timolol digunakan untuk merawat glaukoma. Kedua-duanya diperlukan dalam industri perubatan, tetapi untuk tujuan yang berbeza.
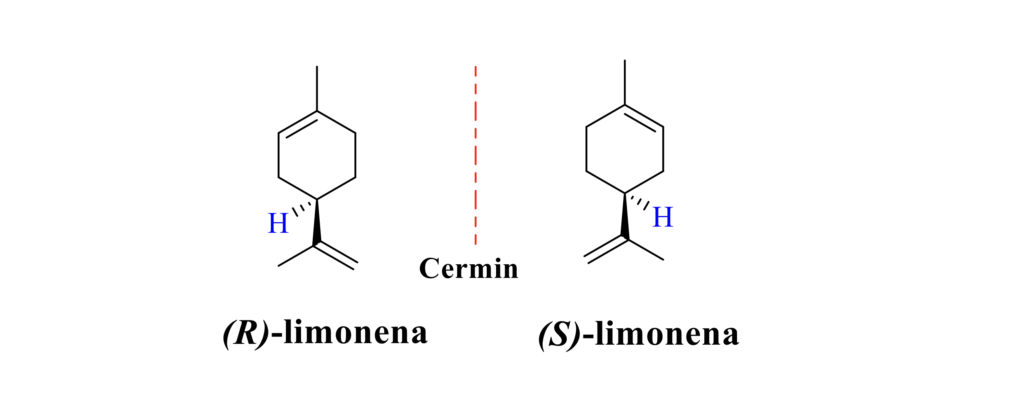
Apakah pula bezanya di antara buah lemon dan oren? Selain warna, tentunya rasa buah tersebut adalah berbeza. Sebenarnya, antara faktor penyumbang kepada rasa oren dan lemon adalah berikutan kehadiran sebatian kimia yang bernama limonena. Limonena turut mempunyai dua isomer di mana isomer (R)-limonena memberikan rasa oren. Manakala, sebatian cerminnya isomer (S)-limonena memberikan rasa lemon pula.
Contoh-contoh yang diberikan adalah sebahagian kecil daripada pelbagai jenis isomer optik sama ada yang wujud secara semulajadi atau disediakan secara sintesis di makmal. Dengan itu, penyelidikan melibatkan isomer optik adalah penting terutamanya bagi membangunkan kaedah pemisahan dua isomer sebatian kimia organik yang mempunyai imej cermin. Hal ini kerana setiap daripadanya mempunyai kesan, aplikasi dan manfaat yang berbeza.
Harus diingat, ianya sama tapi tidak serupa. Begitulah cerita kimia untuk kali ini!
Penulis ialah pensyarah di Jabatan Kimia, Fakulti Sains, Universiti Teknologi Malaysia.